Předměty » Struktura látek (jádro, obal, prvky, vazby…)
Obsah
Látky jsou složeny z částic, které jsou v neustálém pohybu a mohou pronikat mezi částice jiných látek
Pevné látky mají pravidelně uspořádané částice a nazývají se krystalické, pevné látky které netvoří krystal se nazývají beztvaré (amorfní)
Atom
Základní stavební jednotka látek
Zkládá se z kladně nabitého jádra a záporně nabitého obalu
Jádro je složeno z kladně nabitých protonů (p+) a elektricky neutrálních neutronů (n0)
V obalu jsou záporně nabité elektrony (e–)
Atom drží pohromadě díky elektrostatickým silám mezi kladně nabitým jádrem a záporně nabitým obalem
Počet protonů v jádře je vždy shodný s počtem elektronů v obalu, a proto je atom elektricky neutrální
Způsob rozmístění a vzájemného spojení elektronů, protonů a neutronů označujeme jako stavbu neboli strukturu atomu
Jádro atomu
Jádro atomu je 100 000 menší než celý atom
Proton- je mikročástice s nejmenším kladným nábojem
Neutron- je mikročástice bez elektrického náboje
Počet protonů v jádře udává protonové číslo- Z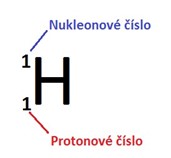
Protony a neutrony se označují nukleony
Počet nukleonů v jádře udává nekleonové číslo A
Nukleony se skládají z meších částic- kvarky, bylo zjištěno šest typů kvarků: horní-u, dolní-d, podivný-s, půvabný-c, vrcholný-t, spodní-b. kvarky se vždy vyskytují v trojcích. Proton- 2 kvarky-u a 1 kvark-d (uud)
Atomy které mají stejný počet protonů i elektronů a liší se pouze počtem neutronů nazýváme izotopy
Obal atomu
Elektron- je mkročástice s nejmenším záporným eleábojem
Elektrony se pohybují v obalu v různých vzdálenostech od jádra v tzv. elektronových Vrstvách. v jednotlivých vrstvách mají elektrony různou energii. nejvzdálenější od jádra je tak zvaná valenční vrstva. elektrony v této vrstvě mají nejvyšší energii. označují se jako valenční elektrony.
Atom může mít 1-7 elektronových vrstev
Počet elektronů v jednotlivých elektronových vrstvách každého atomu je přesně stanoven
Hmotnost protonu i neutronu je mnohonásobně větší než hmotnost elektronu
Chemické prvky
Látka složená z atomů se stejným protonovým číslem se nazývá chemický prvek. Např. všechny atomy s protonovým číslem z=16 jsou atomy prvku síra
Každý chemický prvek je určen:
- Značkou
- Českým a mezinárodním názvem
- Protonovým číslem
O- kyslík- oxygenium- protonové číslo 8
Značky chemických prvků mohou být tvořeny:
- Jedním písmenem: N, C, I, B
- Dvěma písmeny: Na, Fe, Al, Mg
První písmeno se píše velké a druhé malé
Některé mezinárodní názvy prvků označují:
- Vlastnosti prvků- fosfor (světlonoš)
- Výskyt ve sloučeninách- vodík (hydrogenium-osažen ve vodě)
- Stát- polonium (poslko), germanium (německo), gallium (francie)
- Jméno- einsteinium
Periodická soustava prvků (psp)
Ruský chemik dmitrij ivanovič mendělejev utřídil prvky do periodické tabulky na základě zjištění že vlastnosti prvků a jejich sloučenin se pravidelně (periodicky) opakují
Tento jev označujeme jako periodický zákon
Všechny prvky jsou v periodické soustavě prvků uspořádané podle periodického zákona do:
- Period- vodorovných řad- označených čisly 1-7- číslo periody označuje počet elektronových vrstev
- Skupin- svislých sloupců- označených 1-17 nebo I-VIII a písmenem A (hlavní skupiny) a B (vedlejší skupiny). Číslo hlavní skupiny, ve které prvek leží, označuje počet elektronů ve valenční vrstvě tohoto prvku.
Chemické sloučeniny
Chemická vazba
Všechny chemické látky se skládají z atomů
Většina chemických látek se skládá ze sloučených atomů které jsou na sebe vázány silami (chemickou vazbou) a vytvářejí molekuly
Molekula je částice chemické látky složená ze dvou a více atomů
Síly které sojují atomy v molekulách nazýváme chemická vazba
Z molekul je složena většina látek
Chemická vazba vznikne spojením valenčních elektronů
Schopnost atomu přitahovat elektrony chemické vazby se nazývá elektronegativita (X)
Čím vyšší je hodnota X tím více atom přitahuje elektrony chemické vazby ke svému jádru
Typy chemických vazeb
Typy vazeb dělíme podle elektronegativity atomů (∆X) které vazbu tvoří
- Vyzba nepolární- je vazba dvou stejných atomů nebo atomů s rozdílem elektronegativity 0-0,4
- Vazba polární- je vazba mezi atomy s rozdílem elektronegativity 0,4-1,7
- Vazba iontová (silně polární)- je vazba mezi atomy s rozdílem elektronegativity větší než 1,7
Nepolární: H2,O2
Polární: HCl, H2O
Iontová: NaCl, KBr (bromid draselný)
Složení molekul
Některé molekuly jsou složeny z atomů stejného prvku, ale většina molekul se však skládá z atomů různých prvků
Molekula vody H2O se skládá z dvou atomů vodíku a jednoho atomu kyslíku
Chemická látka vzniklá sloučením atomů různých prvků se nazývá chemická sloučenina
Chemické sloučeniny
Chemické látky dělíme na chemické prvky a chemické sloučeniny
Chemická sloučenina je chemická látka vzniklá sloučením atomu dvou nebo více prvků
Sloučenina je vždy tvořena molekulami
Chemické sloučeniny dělíme podle dvou základních hledisek:
- Podle původu
- Anorganické (např. voda, oxid uhličitý, kyselina sírová)
- Organické (např. líh, bílkoviny, vitamíny)
- Podle počtu sloučených prvků
- Dvouprvkové (NaCl, LiF, CO, H2O)
- Tříprvkové (NaOH, HClO, H2SO4)
- Víceprvkové (NaHCO3)
Ionty
Kation
v případě že v průběhu chemické reakce dojde k odtržení jednoho nebo více elektronů z valenční vrstvy vytvoří se z elektro neutrálního atomu částice s kladným nábojem převládá u ní počet protonů v jádře nad počtem elektronů v obalu taková částice se nazývá kation.
Anion
V průběhu chemické reakce může Atom přijmout jeden nebo více elektronů do valenční vrstvy. v tomto případě má vzniklá částice záporný náboj. taková částice se nazývá anion. anionty vznikají z atomu nekovů (Cl–, O2-).
Iontové sloučeniny
Při reakci dvou prvků, které ochotně tvoří ionty se vytvoří kationty a anionty. Ty mají opačný náboj, a proto jsou k sobě poutání velkým elektrostatickými silami. Mezi kationty a anionty se vytváří iontová vazba. Sloučeniny, které jsou částice vázány iontovou vazbou, se nazývají iontové sloučeniny. Patří mezi ně např. chlorid sodný nebo bromid stříbrný.
Vlastnosti:
- Vysoká teplota tání a varu
- Rozpustnost ve vodě
- Tvorba krystalů
- Iontové sloučeniny rozpuštěné nebo roztavené vedou elektrický proud, protože jejich Roztoky obsahují volně pohyblivé ionty.
Chemický vzorec
Chemický vzorec je symbol který udává druh a počet atomů vázaných v molekule. počet atomů v molekule zapisujeme číslicí u značky prvků vpravo dole
Např. H2SO4– dva atomy vodíku, jeden atom síry a čtyři atomy kyslíku
